Pesquisadores do Instituto Alberto Luiz Coimbra, de Pós-Graduação e Pesquisa de Engenharia da Universidade Federal do Rio de Janeiro (Coppe/UFRJ), estão desenvolvendo nanopartículas que sirvam para medicamentos que possam combater os sintomas e os malefícios causados pela covid-19. “A ideia é aumentar a absorção de alguns medicamentos pelo organismo e a disponibilidade para que haja maior eficiência durante o uso visando combater, principalmente, os sintomas”, disse hoje (12), à Agência Brasil, o coordenador do projeto, professor José Carlos Pinto, do Programa de Engenharia Química (PEQ) da Coppe.
Destacou que há atualmente muitas atividades relacionadas ao desenvolvimento dos retrovirais e, inclusive, expectativa de que alguns tratamentos com retrovirais, em um futuro próximo, sejam utilizados. Nesse caso, a tecnologia que se encontra em desenvolvimento pela Coppe poderia ser também utilizada para embarcar esses retrovirais, acentuou.
Ele confirmou que a meta é que os medicamentos a serem desenvolvidos possam ser mais eficientes, dando maior segurança no tratamento contra o novo coronavírus, porque, às vezes, é necessário tomar uma carga de antibióticos elevada que, de certa maneira, agride o organismo do ponto de vista da absorção, em particular os remédios que são tomados via oral.
“Eles agridem o aparelho digestivo. Então, quando vão protegidos por uma espécie de bolinha, o remédio não necessariamente tem contato com as células do estômago. Aí, eles são absorvidos de maneira mais eficiente e de forma também menos agressiva”, afirmou.
Potencialização
Revestidos por nanopartículas feitas de polímero biocompatível (as chamadas bolinhas), esses fármacos poderão ter sua atuação potencializada e seus efeitos adversos e contraindicações reduzidos, o que facilitará o tratamento médico e a reabilitação de pacientes. O projeto, que conta com apoio financeiro da Fundação de Amparo à Pesquisa do Estado do Rio de Janeiro (Faperj), possibilitará o desenvolvimento de medicamentos antivirais mais eficientes e seguros contra o coronavírus.
O professor da Coppe/UFRJ relatou que o grupo de pesquisadores vem trabalhando no sentido de que essas bolinhas sejam inteligentes.
“A gente faz um trabalho de funcionalização. A gente cobre a bolinha com um determinado biocomposto, com uma molécula ou com um agente ativo, como um anticorpo, por exemplo, para que possa fazer a entrega específica para as células que estão afetadas com a doença. Isso possibilita um aumento grande da eficiência, porque é como se as células que estão doentes acabassem absorvendo mais essas bolinhas, que são marcadas com compostos reconhecidos pelas células doentes. Isso também aumenta a eficiência da terapia, porque você entrega um medicamento à célula que mais precisa dele, que é a célula doente, ao invés de espalhar ele pelo organismo”, explicou o professor.
Finalidade
O objetivo é a produção de nanopartículas poliméricas biocompatíveis contendo diferentes fármacos, em especial aqueles que apresentam potencial farmacológico no combate ao Sars-Cov-2, por meio de uma técnica que seja fácil de reproduzir e de produzir em grande escala. O projeto já desenvolveu algumas soluções.
Uma delas inclui a azitromicina, que é um antibiótico que vem sendo muito usado no tratamento da covid, por ele auxiliar a combater, em particular, as infecções no pulmão.
“A gente está em um estágio muito avançado para alguns ativos, como também a heparina, e não tão avançado para outros, como a acetilcisteína e a ivermectina”, disse. O coordenador revelou, ainda, que o grupo de pesquisadores já domina a técnica da funcionalização, mas tem que avançar nos testes in vivo.
Quanto ao desenvolvimento das soluções farmacêuticas, José Carlos confirmou que o projeto está bem avançado. A partir de março do próximo ano, o planejamento é iniciar os testes in vivo em meios celulares. Tudo vai depender do funcionamento dos laboratórios por conta da pandemia.
Formulação
Ele explicou que serão feitos testes, principalmente, em culturas celulares. Deixou claro que o projeto não está apresentando um novo fármaco, mas uma formulação de uma nova apresentação mais inteligente, o que simplifica muito o desenvolvimento do produto final.
“Porque os materiais já são conhecidos. O que não é conhecida é a formulação. É a apresentação. Por isso, a gente tem que fazer testes de fato. Depois de fazer testes com culturas celulares, temos que programar testes com humanos, mas esses testes são mais simples, porque não envolvem compostos novos”, observou.
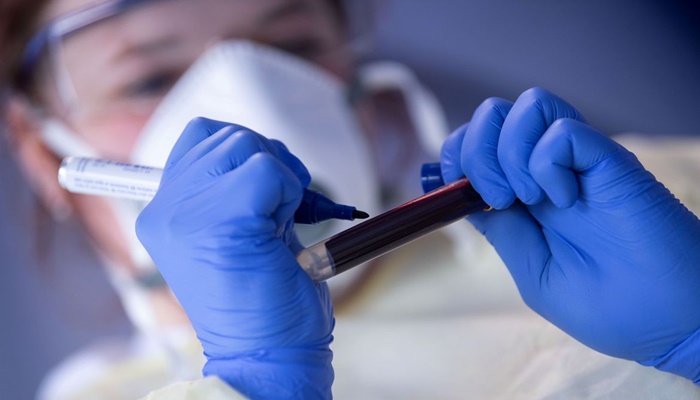
Os testes com culturas celulares envolvem células infectadas com o vírus da covid-19, utilizadas em laboratório. Muitas vezes, são células do epitélio nasal, do intestino, e são colocadas na presença dessas formulações farmacêuticas. O que se pretende com esses testes é validar a internalização de fato dessas bolinhas pelas células e validar o efeito benéfico de absorção para levar o remédio às células infectadas. Não são células de pessoas que morreram de covid, disse o professor. Elas são cultivadas em laboratório.
Dependendo do resultado desses testes e da aprovação pela Comissão de Ética em Pesquisa da UFRJ, poderá ser programado um conjunto de testes com pessoas. “Se o projeto for bem sucedido, a gente imagina que estaria preparado para submeter à Comissão de Ética no prazo de seis meses”. Isso significa que os testes em humanos poderão ser iniciados ainda em 2021.
Outras doenças
José Carlos esclareceu que a tecnologia não é dedicada somente à covid; é uma plataforma que pode ser usada para tratamento de outras doenças. Mesmo que a vacinação dos brasileiros ocorra no início de 2021, a pesquisa não estaria perdida, porque a plataforma de tratamento é genérica e pode ser usada para maximizar o desempenho de medicamentos de maneira geral.
O projeto tem trabalhado com desenvolvimentos similares, embora usando outros medicamentos, outros ativos, para desenvolver soluções para o tratamento do Mal de Alzheimer, da esquistossomose, por exemplo e, inclusive, do câncer.
“O desenvolvimento desta plataforma pode ser muito interessante para o tratamento de outras doenças que não a covid-19, mas que também são causadas pela infecção de células por micro organismos ou que demandem a entrega de medicamentos para células doentes”, especificou.
Fazendo a medicação direcionada e com menores doses do princípio ativo, a técnica pode beneficiar o doente. De acordo com o coordenador, o projeto é um tipo de trabalho que encontra amplo espectro de uso na medicina, de maneira geral.
“Porque esse não é um problema específico da covid-19, mas afeta e está relacionado a uma quantidade grande de doenças e que, funcionando junto com a covid, a gente também constrói a possibilidade dele funcionar com estratégias similares de tratamento”, emendou.
De acordo com o professor, os fármacos usados no tratamento convencional são baratos e servem como ótimos modelos. Em uma segunda etapa, se pretende testar a tecnologia para encapsulação de antivirais e terapia genética, que são fármacos mais complexos e caros. (Com Agência Brasil)
O governo federal entregou no sábado (12), ao Supremo Tribunal Federal (STF), o plano nacional de imunização contra a covid-19. O documento foi entregue pelo advogado-geral da União, José Levi, ao ministro Ricardo Lewandovski, relator das ações que tratam da obrigatoriedade da vacina e outras medidas de combate à pandemia.
Batizado de Plano Nacional de Operacionalização da Vacinação contra a Covid-19, o documento foi elaborado pelo Ministério da Saúde, possui 93 páginas e está dividido em dez eixos, que incluem descrições sobre a população-alvo para a vacinação, as vacinas já adquiridas pelo governo e as que estão em processo de pesquisa, a operacionalização da imunização, o esquema logístico de distribuição das vacinas pelo país e as estratégias de comunicação para uma campanha nacional. O documento não indica data para início da vacinação.
Vacinas
Segundo o plano, o governo federal já garantiu 300 milhões de doses de vacinas contra a covid-19 por meio de três acordos:
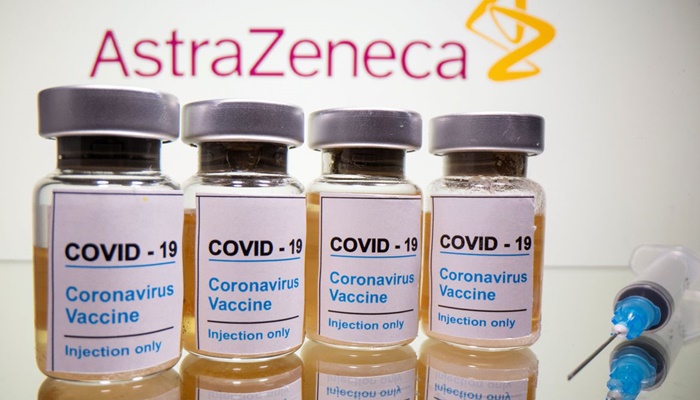
- Fiocruz/AstraZeneca - 100,4 milhões de doses até julho/2020 + 30 milhões de doses/mês no segundo semestre;
- Covax Facility - 42,5 milhões de doses;
- Pfizer - 70 milhões de doses (em negociação);
Até agora, nenhum imunizante está registrado e licenciado pela Agência Nacional de Vigilância Sanitária (Anvisa), etapa prévia obrigatória para que a vacinação possa ser realizada.
"De acordo com o panorama da OMS [Organização Mundial da Saúde], atualizado em 10 de dezembro de 2020, existem 52 vacinas covid-19 candidatas em fase de pesquisa clínica e 162 candidatas em fase pré-clínica de pesquisa. Das vacinas candidatas em estudos clínicos, há 13 em ensaios clínicos fase 3 para avaliação de eficácia e segurança, a última etapa antes da aprovação pelas agências reguladoras e posterior imunização da população. No Brasil, o registro e licenciamento de vacinas é atribuição da Agência Nacional de Vigilância Sanitária (Anvisa), pautados na Lei nº 6.360/1976 e regulamentos técnicos como a RDC nº 55/2010", diz um trecho do plano.
Grupos prioritários
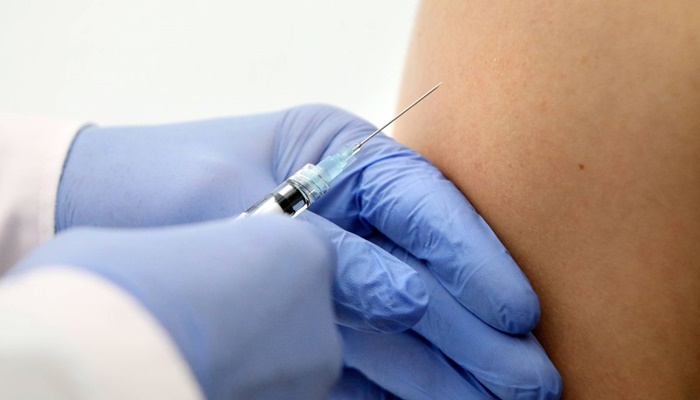
O Plano Nacional de Vacinação contra a covid-19, apresentado pelo governo, prevê quatro grupos prioritários que somam 50 milhões de pessoas, o que vai demandar 108,3 milhões de doses de vacina, já incluindo 5% de perdas, uma vez que cada pessoa deve tomar duas doses em um intervalo de 14 dias entre a primeira e a segunda injeção.
O primeiro grupo prioritário, a ser vacinado na fase 1, é formado por trabalhadores da saúde (5,88 milhões), pessoas de 80 anos ou mais (4,26 milhões), pessoas de 75 a 79 anos (3,48 milhões) e indígenas com idade acima de 18 anos (410 mil). A fase 2 é formada por pessoas de 70 a 74 anos (5,17 milhões), pessoas de 65 a 69 anos (7,08 milhões), pessoas de 60 a 64 anos (9,09 milhões).
Na fase 3, a previsão é vacinar cerca de 12,66 milhões de pessoas acima dos 18 anos que tenham as seguintes comorbidades: hipertensão de difícil controle, diabetes mellitus, doença pulmonar obstrutiva crônica, doença renal, doenças cardiovasculares e cerebrovasculares, indivíduos transplantados de órgão sólido, anemia falciforme, câncer e obesidade grave (IMC maior ou igual a 40).
Na fase 4, deverão ser vacinados professores do nível básico ao superior (2,34 milhões), forças de segurança e salvamento (850 mil) e funcionários do sistema prisional (144 mil). O Ministério da Saúde pondera, no documento, que os grupos previstos ainda são preliminares e poderão ser alterados.
"Vale ressaltar que os grupos previstos são preliminares, passíveis de alteração a depender das indicações da vacina após aprovação da Anvisa, assim como as possíveis contraindicações. Destaca-se ainda que há outros grupos populacionais considerados prioritários, a serem incluídos dentre as fases apresentadas, discutidos no âmbito da câmara técnica, a exemplo das populações ribeirinhas e quilombolas, cuja estimativa populacional está em atualização pelo Instituto Brasileiro de Geografia e Estatística (IBGE), para avaliação de qual fase esses grupos estarão inseridos, de acordo com o cenário de disponibilidade de vacinas e estratégia de vacinação", diz o plano.
Também de acordo com o plano, o registro da dose da vacina aplicada será feito de forma nominal e individualizada, diretamente no Sistema de Informação do Programa Nacional de Imunizações (SI-PNI) em todos os pontos de vacinação da rede pública e privada de saúde. O ministério trabalha com a implantação de um sistema informatizado para monitorar e controlar os dados de vacinação.
"Uma solução tecnológica está em desenvolvimento, por meio do Datasus, com o objetivo de simplificar a entrada de dados e agilizar o tempo médio de realização do registro do vacinado no SI-PNI, além de considerar aspectos de interoperabilidade com outros Sistemas de Informação e integração com a Rede Nacional de Dados em Saúde (RNDS). Um recurso que será colocado à disposição é o QR-Code para identificar o cidadão a ser vacinado. Este deverá ser gerado pelo próprio cidadão no Aplicativo Conecte SUS".
Logística
Para operacionalizar a campanha nacional de vacinação, o plano do governo prevê capacitação dos profissionais de saúde do SUS e também um esquema de recebimento, armazenamento, expedição e distribuição dos insumos, que são o próprio imunizante, além das seringas e agulhas.
O principal complexo logístico será a partir do aeroporto internacional de Guarulhos (SP), na sede da empresa VTC Logística, que tem contrato com o Ministério da Saúde. O galpão da empresa possui 36 mil metros quadrados nas imediações do aeroporto e conta com ambientes climatizados, como docas e câmaras frias. Há também estruturas menores em Brasília, Rio de Janeiro e Recife.
Também está prevista a entrega da carga embalada por modal rodoviário para estados como Santa Catarina, Espírito Santo, Mato Grosso do Sul, Goiás, Distrito Federal, Rio Grande do Sul, Minas Gerais e outros que fiquem em até 1.400 quilômetros de raio dos centros de distribuição.
O governo também informa já ter acordos firmados com companhias aéreas, como Latam e Azul, além de outras empresas de carga aérea, para o transporte até as capitais da região Norte do país. Pelo plano, a frota será rastreada 100% por satélite e a segurança do transporte, em determinadas situações durante o deslocamento, ocorrerá por conta da União.
Orçamento
Ainda de acordo com o plano, o governo federal já disponibilizou R$ 1,9 bilhão de encomenda tecnológica associada à aquisição de 100,4 milhões de doses de vacina pela AstraZeneca/Fiocruz e R$ 2,5 bilhões para adesão ao Consórcio Covax Facitity, associado à aquisição de 42 milhões de doses de vacinas.
Além disso, outros R$ 177,6 milhões para custeio e investimento na Rede de Frio, na modernização dos Centros de Referência para Imunobiológicos Especiais (CRIEs), no fortalecimento e ampliação da vigilância de síndromes respiratórias. Também, segundo a pasta, outros R$ 62 milhões foram investidos para aquisição de mais 300 milhões de seringas e agulhas. (Com Agência Brasil)
A Agência Nacional de Vigilância Sanitária (Anvisa) encerra hoje (11) a inspeção presencial iniciada no dia 7 na empresa chinesa Wuxi Biologics, responsável pela fabricação de insumos ativos biológicos usados pela Fiocruz para a produção da vacina AstraZeneca/Oxford.
A partir de agora, os inspetores designados pela Anvisa enviados à China para verificar se a empresa tem adotado práticas adequadas para a fabricação dos insumos aguardam manifestação da Wuxi Biologics, em resposta a algumas informações adicionais decorrentes da inspeção, para emitirem o relatório. Só então o processo de certificação será concluído.
Em nota, a Anvisa informa que a previsão é de que a certificação em boas práticas de fabricação ocorra entre a primeira e segunda semanas de janeiro.
Ontem (10), a Anvisa aprovou, por meio de deliberação de sua Diretoria Colegiada, a resolução que “abre possibilidade aos laboratórios de solicitarem autorização para uso emergencial, em caráter experimental, de vacinas contra covid 19”.
A decisão oficializa o pedido de uso emergencial de vacina anunciado no dia 2 de dezembro pela própria Anvisa. (Com Agência Brasil)
As inscrições para o Exame Nacional do Ensino Médio para Pessoas Privadas de Liberdade, ou sob medida socioeducativa que inclua privação de liberdade (Enem PPL) 2020 foram prorrogadas até o dia 18 deste mês. Agora, o responsável pedagógico de cada unidade prisional ou socioeducativa terá mais uma semana para fazer o registro dos participantes.
Antes da mudança, as inscrições terminariam nesta sexta-feira (11).
As provas do Enem PPL 2020 serão aplicadas nos dias 23 e 24 de fevereiro de 2021. As unidades deverão garantir a segurança e o sigilo da aplicação do exame dentro dos locais de prova indicados. As unidades prisionais precisam ainda ter um espaço de ambiente escolar coberto, silencioso, com iluminação, mesas e cadeiras em condições para a realização do exame.
Além de fazer as inscrições, o responsável pedagógico deve determinar as salas de provas dos participantes e a transferência entre as unidades, quando necessário, dentro do prazo previsto, e excluir aqueles que tiverem sua liberdade decretada.
O profissional terá acesso aos resultados obtidos pelos participantes e ao Sistema de Seleção Unificada (Sisu) para pleitear uma vaga na educação superior. Também ficará a cargo desse colaborador a divulgação das informações sobre o exame aos participantes privados de liberdade.
Idade
Candidatos com idade a partir de 18 anos poderão usar o desempenho no Enem como mecanismo único, alternativo ou complementar para acesso à educação superior. Já os menores de 18 anos, que fazem a prova com o intuito de conhecer a avaliação e não têm ensino médio completo — “treineiros” —, só poderão usar os resultados individuais no exame para autoavaliação de conhecimentos.
Na edição do ano passado, o Enem PPL recebeu 46.240 inscrições, com 1.228 instituições homologadas para a aplicação da prova em 25 estados e no Distrito Federal. O estado de São Paulo teve o maior número de inscrições - 15.826 -, seguido de Minas Gerais: 4.959.
Covid-19
Todos os candidatos ao Enem 2020 que forem diagnosticados com alguma doença infectocontagiosa, como a covid-19 e, portanto, estiverem impossibilitados de fazer as provas por este motivo, poderão participar da reaplicação da prova no mesmo dia das pessoas privadas de liberdade.
Nesse caso, a orientação é ligar para a central de atendimento do Instituto Nacional de Estudos e Pesquisas Educacionais Anísio Teixeira (Inep), no telefone 0800 616161, e comunicar a doença até um dia antes da data da prova.
Além disso, depois da aplicação, o candidato deverá registrar o problema anexando laudo médico na página do participante.
Outras doenças
Além da covid-19, o edital prevê na lista para reaplicação da prova casos de coqueluche, difteria, doença invasiva por Haemophilus influenza, doença meningocócica e outras meningites, varíola, influenza humana A e B, poliomielite por poliovírus selvagem, sarampo, rubéola e varicela.
Com exceção de pessoas com problemas de saúde na data das provas, quem tiver problemas logísticos, como, por exemplo, falta de energia elétrica também poderá comunicar o problema pela Página do Participante para fazer o exame em fevereiro. (Com Agência Brasil)
A partir de agora, associados do Sicredi no Brasil inteiro poderão aproveitar mais um benefício proporcionado pela instituição financeira por meio de suas soluções de pagamento. Trata-se da Tag de Passagem do Sicredi, serviço para utilização em cancelas automáticas, como as de pedágios rodoviários e, em breve, em estacionamentos também, sem a necessidade de parar e realizar o pagamento manualmente.
Com o produto, um adesivo com chip que é colado no automóvel, o usuário terá a conveniência de passar pelas cancelas de cobrança tendo o valor debitado direto de sua conta corrente, evitando filas e com maior segurança. A Tag de Passagem do Sicredi é oferecida por meio de uma parceria com a empresa Green Pass, proprietária da marca Taggy e que possui acessos em pontos de pedágio de 298 municípios, em sua maioria localizados nas regiões Sul, Sudeste e Centro-oeste do país.
“Estamos sempre buscando evoluir em nossas soluções eletrônicas de pagamento para proporcionar mais conveniência ao associado. Nesse sentido, nos mantemos atentos às tendências e oportunidades de conexão com empresas que possamos desenvolver parcerias. A Tag de passagem é um exemplo disso e traduz um pouco do que é a visão de futuro do Sicredi, com as soluções digitais a serviço das pessoas, cada vez mais opções e formas de pagamentos e, por consequência, mais benefícios aos nossos associados”, afirma a gerente de Produtos de Emissão do Sicredi, Solange Parisoto.
A novidade será oferecida aos associados pessoa física e somente poderá ser usada em carros de passeio com dois eixos. Os interessados em adquirir a Tag de passagem podem solicitá-la nas agências do Sicredi. Após a ativação e uso, as transações poderão ser conferidas de maneira simples pelo aplicativo do Sicredi.
Realizado na noite desta quinta-feira (10) em São Paulo, o sorteio 2.326 da Mega-Sena acumula um prêmio de cerca de R$ 34 milhões para os felizardos que acertarem as 6 dezenas. Confira os números sorteados:
10 - 16 - 27 - 34 - 36 - 57
Segundo informou a Caixa, nenhuma aposta acertou as 6 dezenas. A quina, entretanto, teve 55 vencedores - cada um receberá R$ 45.721,34. Já a quadra teve 3.883 vencedores - cada um receberá R$ 925,15.
O sorteio de hoje é o 2º da chamada Mega-Semana de Natal. A Caixa sorteará no próximo sábado (12) outro prêmio, de valor ainda não divulgado. As apostas podem ser feitas em casas lotéricas ou pela internet até às 19h do dia do concurso. As apostas custam R$ 4,50 por 6 dezenas em cada bilhete.
Para apostas com mais dezenas, até o limite de 15, o valor individual do bilhete pode chegar a R$ 22.522,50. As chances de acerto para a aposta com 15 dezenas são de 1 em 10.003.
*Matéria atualizada às 22h04 para acréscimo de informações da Caixa. (Com Agência Brasil)