A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou a possibilidade de produção de vacinas contra a covid-19 em uma fábrica da empresa Hospira, no estado de Kansas, nos Estados Unidos. A medida é necessária para que o imunizante seja usado no Brasil.
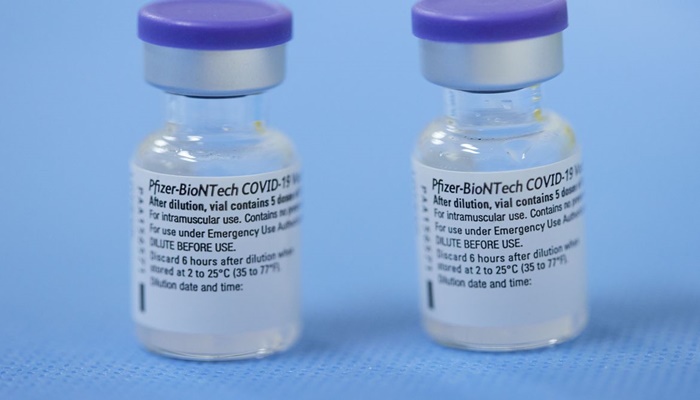
A unidade poderá ser utilizada na fabricação de doses da vacina desenvolvida pelo consórcio da Pfizer e da BioNTech, que já recebeu autorização para uso no Brasil e que teve contrato de aquisição de 200 milhões de doses neste ano com o Ministério da Saúde.
A autorização reconheceu o que a agência chama de “boas práticas de fabricação” da planta produtiva. Este é uma das exigências para que uma fábrica possa ser incluída no registro de um imunizante e possa ser utilizada no seu processo produtivo.
Com isso, o consórcio Pfizer/BioNTech pode ampliar a capacidade de fabricação de doses, o que abre espaço para acelerar a disponibilização de lotes para o Brasil.
Sputnik V
Hoje a Anvisa também disponibilizou para assinatura os termos de compromisso com governos do Nordeste que adquiriram lotes da vacina russa Sputnik V. Os termos fazem parte das exigências definidas pela agência quando da autorização da importação excepcional do imunizante.
Deverão assinar os termos os estados que importaram lotes do imunizante: Bahia, Maranhão, Sergipe, Ceará, Pernambuco, Piauí, Rio Grande do Norte, Alagoas e Paraíba. Além desta obrigação, outros condicionantes foram determinados pela Anvisa para o uso da Sputnik V.
Entre eles estão a submissão de documentos e insumos ao Instituto Nacional de Controle de Qualidade em Saúde da Fiocruz para análise das amostras; submissão à agência de medidas de mitigação de risco pela ausência de validação de uma das fases no exame do pedido de importação e envio à Anvisa do relatório final de produção do Insumo Farmacêutico Ativo (IFA).
Segundo a Anvisa, a análise pelo instituto da Fiocruz é condição sem a qual as vacinas não poderão ser aplicadas na população. A partir do momento que tiver início a aplicação, deverá haver um acompanhamento pelas autoridades de saúde dos estados com estudos de efetividade. (Com Agência Brasil)
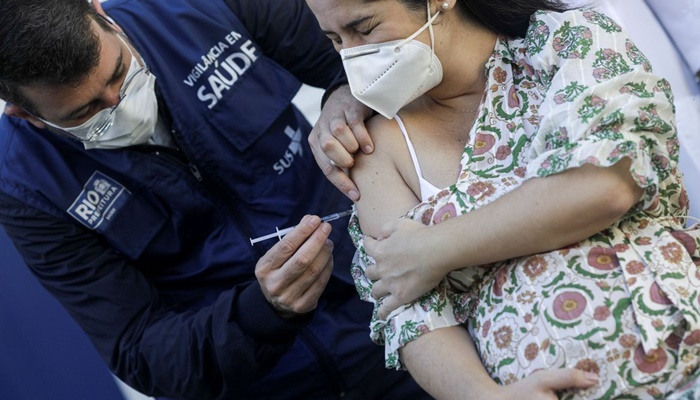
A Câmara dos Deputados aprovou nesta quinta-feira (8) o projeto de lei que inclui gestantes, lactantes e puérperas grupo prioritário no Plano Nacional de Imunização (PNI) para vacinação contra a covid-19. A matéria será enviada à sanção presidencial.
Oriundo do Senado, o texto estabelece ainda que crianças e adolescentes com deficiência permanente ou com comorbidade e adolescentes privados de liberdade também serão incluídos como prioritários no PNI. Essa medida, porém, depende de registro ou autorização de uso emergencial de vacinas no Brasil para pessoas com menos de 18 anos.
Atualmente, a vacina da Pfizer/BioNTech é a única liberada pela Agência Nacional de Vigilância Sanitária (Anvisa) para aplicação em adolescentes com mais de 12 anos.
Risco
A relatora do projeto foi a deputada Luisa Canziani (PTB-PR), que recomendou a aprovação do texto do Senado, com uma emenda de redação. O trecho ressalta a competência do Ministério da Saúde de regulamentar a priorização da vacinação das gestantes, puérperas e lactantes.
“Às lactantes também deve ser garantido o direito de vacinação com prioridade. A sua imunização não apenas permite que os anticorpos produzidos pela mãe passem para os bebês, por meio da amamentação, como também diminui a chance da mãe que retorna ao trabalho pegar a doença e contaminar o filho”, argumentou a congressista.
Outros grupos
Segundo o plano de imunização do Ministério da Saúde, há cerca de 30 categorias separadas por risco de gravidade dos sintomas e de contágio. Depois dos idosos acima de 60 anos, vêm indígenas, pessoas com deficiência permanente, moradores de rua e presidiários, por exemplo. Entretanto, estados e municípios têm autonomia para incluir ou mudar categorias em seus planos de imunização. (Com Agência Brasil)
Mais de 110 milhões de doses de vacinas contra a covid-19 já foram aplicadas no Brasil, o que significa que mais da metade da população vacinável já receberam pelo menos uma dose de imunizante, ou seja, mais de 80 milhões de pessoas.
No país, considera-se público vacinável pessoas maiores de 18 anos, correspondendo a cerca de 160 milhões de brasileiros. Já foram distribuídas, pelo Ministério da Saúde, mais 143 milhões de doses de vacinas para os estados e o Distrito Federal, possibilitando a imunização de 100% dos grupos prioritários da campanha, com pelo menos uma dose da vacina.
O ministro da Saúde, Marcelo Queiroga, disse que essa marca vai além dos números. “Os efeitos da nossa campanha de vacinação podem ser percebidos na redução de óbitos e de internações decorrentes da doença. Estamos no caminho certo para salvar cada vez mais vidas”.
O ministro ressaltou a importância de a população completar o esquema vacinal com as duas doses dos imunizantes. “A melhor vacina é aquela aplicada no braço do brasileiro. E, para que ela tenha o efeito desejado, é preciso que a pessoa vá até o local de vacinação no prazo correto e tome a segunda dose. Só assim a imunização estará completa”, disse.
Nessa quarta-feira (7), o ministério lançou campanha para incentivar a vacinação com a segunda dose do imunizante. Entre as vacinas liberadas pela Agência Nacional de Vigilância Sanitária (Anvisa), para serem aplicadas no Brasil, estão a AstraZeneca/Fiocruz, Pfizer/BioNTech e Coronavac/Butantan. Apenas a Janssen, da farmacêutica Johnson & Johnson, é dose única. (Com Agência Brasil)
Trabalhadores informais e inscritos no Cadastro Único para Programas Sociais do Governo Federal (CadÚnico) nascidos em junho podem sacar, a partir de hoje (9) a terceira parcela do auxílio emergencial 2021. O dinheiro foi depositado nas contas poupança digitais da Caixa Econômica Federal em 24 de junho.

Os recursos também poderão ser transferidos para uma conta-corrente, sem custos para o usuário. Até agora, o dinheiro apenas podia ser movimentado por meio do aplicativo Caixa Tem, que permite o pagamento de contas domésticas (água, luz, telefone e gás), de boletos, compras em lojas virtuais ou compras com o código QR (versão avançada do código de barras) em maquininhas de estabelecimentos parceiros.
Em caso de dúvidas, a central telefônica 111 da Caixa funciona de segunda a domingo, das 7h às 22h. Além disso, o beneficiário pode consultar o site auxilio.caixa.gov.br.
Originalmente, o saque estava previsto para ocorrer em 27 de julho, mas foi antecipado em quase três semanas por decisão da Caixa. Segundo o banco, a adaptação dos sistemas tecnológicos e dos beneficiários ao sistema de pagamento do auxílio emergencial permitiu o adiantamento do calendário.
O auxílio emergencial foi criado em abril do ano passado pelo governo federal para atender pessoas vulneráveis afetadas pela pandemia de covid-19. Ele foi pago em cinco parcelas de R$ 600 ou R$ 1,2 mil para mães chefes de família monoparental e, depois, estendido até 31 de dezembro de 2020 em até quatro parcelas de R$ 300 ou R$ 600 cada.
Neste ano, a nova rodada de pagamentos, durante quatro meses, prevê parcelas de R$ 150 a R$ 375, dependendo do perfil: as famílias, em geral, recebem R$ 250; a família monoparental, chefiada por uma mulher, recebe R$ 375; e pessoas que moram sozinhas recebem R$ 150.
Regras
Pelas regras estabelecidas, o auxílio será pago às famílias com renda mensal total de até três salários mínimos, desde que a renda por pessoa seja inferior a meio salário mínimo. É necessário que o beneficiário já tenha sido considerado elegível até o mês de dezembro de 2020, pois não há nova fase de inscrições. Para quem recebe o Bolsa Família, continua valendo a regra do valor mais vantajoso, seja a parcela paga no programa social, seja a do auxílio emergencial. (Com Agência Brasil)
O prazo para adesão das instituições de educação superior públicas ao Sistema de Seleção Unificada (Sisu) termina nesta sexta-feira (9), às 23h59. A adesão refere-se à segunda edição de 2021.
O edital com cronograma e procedimentos, que valem tanto para instituições federais quanto estaduais ou municipais, foi publicado no Diário Oficial da União, na segunda-feira (5), pelo Ministério da Educação (MEC).
O Sisu é o programa do MEC para acesso de brasileiros a cursos de graduação em universidades públicas do país. As vagas são abertas semestralmente, por meio de um sistema informatizado.
O processo seletivo do Sisu para o segundo semestre de 2021 está previsto para ocorrer em agosto. (Com Agência Brasil)
A Diretoria da Agência Nacional de Vigilância Sanitária (Anvisa) aprovou em reunião hoje (7) a prorrogação de regras especiais para a comercialização de medicamentos e vacinas utilizados em pacientes acometidos pela covid-19.
Os diretores estenderam por mais dois meses a vigência da Resolução nº 483 de 2021, que trata da importação de vacinas, considerando permissões e registros dados por autoridades sanitárias de outros países. Essa alternativa, prevista na Lei nº 14.124 de 2021, foi utilizada, por exemplo, para a liberação, com condicionantes, das importações das vacinas Covaxin e Sputnik V pela agência.
O relator da matéria, o diretor da Anvisa Alex Campos, justificou a concordância com a prorrogação pela continuidade da emergência de saúde causada pela pandemia e pela necessidade de garantia de mais doses para o Brasil como forma de acelerar a campanha de imunização.
“O que trazemos hoje é a prorrogação de mais 60 dias, esperando que este seja o último período de importações com essa modalidade regulatória. Mas faremos avaliações no decorrer deste prazo e uma próxima prorrogação pode ser analisada pela Diretoria da Anvisa”, analisou Campos.
A diretora da agência Cristiane Jourdan adotou postura semelhante e lembrou que essas flexibilizações foram adotadas para facilitar o combate à pandemia no Brasil, desafio que ainda se coloca no momento atual.
“A resolução integra conjunto de medidas para ampliar a oferta de medicamentos e produtos de saúde para pacientes acometidos com a pandemia. Essa prorrogação se mostra necessária considerando os benefícios à sociedade. O contexto atual da pandemia no Brasil ainda é semelhante ao momento de quando a norma foi editada", explicou.
Medicamentos para intubação
A Diretoria da Anvisa também ampliou, dessa vez até o fim do ano, a vigência da Resolução nº 484 de 2021, que flexibilizou as exigências para comercialização de medicamentos adotados na internação de pessoas com covid-19, que fazem parte do que passou a ser chamado popularmente de “kit intubação”.
A norma isentou esses medicamentos da necessidade de registro. Os fabricantes passaram a poder apenas notificar a agência. Outra permissão foi a possibilidade pelas empresas de alterar o medicamento sem uma autorização prévia.
Assim como na resolução anterior, a avaliação dos diretores foi que a persistência da pandemia mantém o problema das internações e da pressão sobre os sistemas de saúde, criando risco de desabastecimento desses medicamentos.
“Apesar dos sinais positivos da campanha vacinal, o cenário pandêmico nos mantém em alerta e vem persistindo, levando a pressão sobre o sistema de saúde, bem como o persistente risco de desabastecimento de insumos estratégicos para o enfrentamento à pandemia no Brasil”, concluiu a diretora da Anvisa Meiruze Freitas, relatora do caso.
De acordo com ela, até o momento foram notificados nove medicamentos utilizados para procedimentos de internação de pacientes com covid-19. Outros dois fabricantes comunicaram mudanças em seus produtos. “Não foram protocoladas reclamações ou relatos de problemas relacionados a esses medicamentos”, acrescentou Freitas.
“A prorrogação deste prazo é coerente com a atual situação da pandemia, com as informações que temos colhido de maneira permanente, com o cuidado do regulador não ser agente de desequilíbrio do sistema de fornecimento”, reforçou o diretor da agência Alex Campos. (Com Agência Brasil)















-PortalCantu-19-04-2026_large.png)



