A Agência Nacional de Vigilância Sanitária (Anvisa) proibiu a comercialização de alguns lotes da fórmula infantil em pó Nutramigen LGG, da marca Enfamil, fabricado pela empresa Reckitt/Mead Johnson Nutrition, dos Estados Unidos. A medida é preventiva, já que não foi identificada a exportação dos respectivos lotes ao Brasil. 

De acordo com a Anvisa, a agência sanitária norte-americana (Food and Drug Administration - FDA) emitiu comunicado relacionado ao recolhimento voluntário pela empresa, nos Estados Unidos, de lotes do produto, devido a uma possível contaminação da fórmula em pó pela bactéria Cronobacter sakazakii. “A forma clínica mais frequente da infecção por Cronobacter spp. é a meningite, podendo ocorrer outras complicações como enterocolite necrosante, bacteremia, septicemia e sequelas irreversíveis”, alertou a agência brasileira.
Os lotes atingidos são: ZL3FHG, ZL3FMH, ZL3FPE, ZL3FQD, ZL3FRW e ZL3FX. Eles têm código de barras 300871239418 ou 300871239456 e prazo de validade até 01/01/2025.
A resolução com a proibição foi publicada nesta sexta-feira (12) no Diário Oficial da União.
Os últimos dados divulgados pela FDA informam que esses produtos foram exportados para Argentina, Bélgica, Belize, Canadá, Colômbia, Costa Rica, República Dominicana, Equador, El Salvador, Guatemala, Irlanda, Israel, Jamaica, México, Nicarágua, Peru, Polônia, Espanha, Reino Unido e Venezuela.
Segundo a Anvisa, com informações fornecidas pela FDA e pela Reckitt/Mead Johnson Nutrition, não foram identificados casos de infecções até o momento relacionados ao consumo desses lotes do produto.
Orientações
A Anvisa orienta aos consumidores que utilizam produtos Nutramigen LGG que verifiquem o lote impresso no rótulo do produto. “Se o produto pertencer a um dos lotes recolhidos, ele não deve ser utilizado ou oferecido para o consumo por bebês”, alerta.
“Somente utilize fórmulas infantis com orientação de um profissional de saúde habilitado, como médico pediatra ou nutricionista. O Ministério da Saúde e a Organização Mundial da Saúde (OMS) recomendam o aleitamento materno até os dois anos de idade ou mais e de maneira exclusiva até os seis meses de vida”, acrescenta a Anvisa.
Segundo a agência, a correta higienização de utensílios que entram em contato com a fórmula, como mamadeiras, copos e colheres, é fundamental para garantir a segurança do produto. Além disso, deve-se sempre realizar a diluição na quantidade adequada e na temperatura segura (70ºC), que garante o menor risco de contaminação por microrganismos perigosos, como bactérias do gênero Cronobacter e Salmonella.
A Cronobacter sakasakii é uma bactéria pertencente ao gênero Cronobacter spp. e pode causar infecções em humanos, principalmente em recém-nascidos, bebês prematuros de baixo peso (menos de 2,5 quilos), imunocomprometidos e prematuros que necessitam de cuidados especiais na Unidade de Terapia Intensiva (UTI) neonatal.
A Anvisa explicou ainda que esse grupo de bactérias pode afetar também indivíduos de outras faixas etárias, entretanto, casos envolvendo adultos e crianças com idade superior a 1 ano são raros. A taxa de mortalidade é elevada nos grupos de risco.
Registro no Brasil
Fórmulas infantis são alimentos que necessitam de registro na Anvisa para serem comercializados. O número desse registro deve constar no rótulo do produto.
Atualmente, as fórmulas infantis Nutramigen LGG registradas na Anvisa possuem a seguinte denominação: fórmula infantil de seguimento para lactentes destinada a necessidades dietoterápicas especiais com restrição de lactose composta por proteína extensamente hidrolisada e probiótico.
Esses produtos são importados sob responsabilidade da Mead Johnson do Brasil Comércio e Importação de Produtos de Nutrição Ltda. (CNPJ: 10.351.637/0001-86) e são provenientes dos Estados Unidos (registro 6.6609.0032.001-4) e do México (registro 6.6609.0032.002-2).
“O consumidor deve ficar atento e somente adquirir produtos com procedência conhecida e registrados na Anvisa. Produtos importados não registrados são considerados irregulares”, alertou a agência. “Recomenda-se também que os consumidores evitem comprar fórmulas infantis importadas por meio de comércio eletrônico, devido à dificuldade em conhecer a origem e a regularidade do produto”, acrescentou.
Para confirmar o registro do produto, é possível consultar a base de dados disponível no portal da Anvisa..
por Agência Brasil
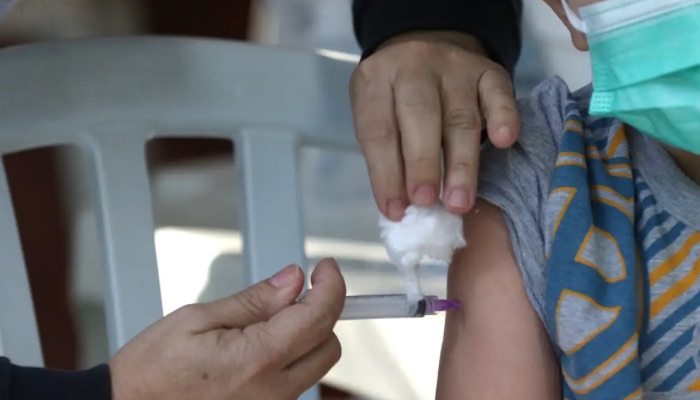
A Sociedade Brasileira de Imunizações (SBIm) divulgou nessa quinta-feira (11) posicionamento em que critica uma pesquisa conduzida pelo Conselho Federal de Medicina (CFM) para saber a opinião dos médicos sobre a obrigatoriedade da vacinação de crianças de 6 meses a menos de 5 anos contra a covid-19.

No formulário disponível, o CFM alega que está conduzindo a pesquisa "para entender a percepção dos médicos brasileiros" sobre a obrigatoriedade da imunização de crianças, e afirma que a opinião dos profissionais "é fundamental para enriquecer a análise e contribuir para a tomada de decisões futuras".
Para a SBIm, a pesquisa equipara as crenças pessoais dos médicos à ciência, o que pode gerar insegurança na comunidade médica e afastar a população das salas de vacinação.
"A SBIm entende que a pesquisa realizada pelo Conselho Federal de Medicina (CFM) não trará nenhum benefício à sociedade", afirma instituição científica.
Mortes por covid-19
A SBIM lembra que a covid-19 foi responsável por 5.310 casos de síndrome respiratória aguda grave (SRAG) e 135 mortes entre crianças menores de 5 anos no Brasil em 2023, de acordo com o último boletim epidemiológico do Ministério da Saúde, que reúne dados até novembro.
Além disso, desde o início da pandemia, houve 2.103 casos de Síndrome Inflamatória Multissistêmica Pediátrica (SIM-P), considerada uma manifestação tardia da covid-19, com 142 mortes.
Diante disso, a sociedade ressalta que a vacinação contra a covid-19 é uma estratégia comprovadamente eficaz e segura para a prevenção da doença, potencialmente fatal também entre crianças.
A segurança da vacina é reforçada pelo último boletim de monitoramento de Eventos Supostamente Atribuíveis à Vacinação e à Imunização (Esavi) publicado pelo Ministério da Saúde. Segundo o documento, após a aplicação de mais de 47 milhões de doses em pessoas menores de 18 anos, entre 18 de janeiro de 2021 e 31 de dezembro de 2022, a grande maioria dos eventos propriamente ditos foram leves ou moderados, como dor de cabeça, febre, dor muscular e outras reações esperadas.
Além disso, a SBIM argumenta que o Brasil dispõe de pelo menos dois dispositivos legais que estabelecem a obrigatoriedade da vacinação de menores de 18 anos, os artigos 227 da Constituição Federal e 14 do Estatuto da Criança e do Adolescente (ECA), que determina em parágrafo único que "é obrigatória a vacinação das crianças nos casos recomendados pelas autoridades sanitárias".
Resposta
Em texto com título de "Nota aos Brasileiros", o CFM afirma que em nenhum momento contestou a decisão de disponibilizar a vacina contra a covid-19 para a população infantil. O conselho diz que sua pesquisa decorre de inúmeros pleitos encaminhados à autarquia e visa apenas conhecer a "percepção do médico brasileiro sobre a obrigação imposta aos pais para que as crianças de 6 meses a 4 anos e 11 meses sejam vacinadas, independentemente de prescrição médica da vacina contra covid-19".
O CFM acrescenta que já realizou consultas sobre outros assuntos e defende que "os médicos têm opiniões com base em conhecimento técnico-científico, são profissionais, pesquisadores e estudiosos em diversas áreas da ciência médica e por isso mesmo, são capacitados a se manifestarem".
Sobre a nota da SBIM, o conselho afirma que "respeita o direito de outras entidades médicas se posicionarem sobre a realização da pesquisa, entendendo que essas manifestações enriquecem o debate ético e científico, desde que não atendam a interesses pessoais, políticos, ideológicos ou financeiros".
A autarquia conclui dizendo que empenha total apoio às ações empreendidas para ampliar "a cobertura de vacinas que ajudam na prevenção e combate a doenças", citando como exemplos as de poliomielite, sarampo, meningite, rubéola e tuberculose.
*texto atualizado às 15h41 para acréscimo de resposta do Conselho Federal de Medicina
Por Agência Brasil
Os corpos dos quatro ocupantes do helicóptero que desapareceu há 12 dias em São Paulo foram encontrados junto à aeronave. A Polícia Militar (PM) encontrou os destroços em uma mata fechada no município de Paraibuna, no Vale do Paraíba. O aparelho foi localizado pelo Águia 24, da PM. Equipes de resgate estão no local.
O helicóptero saiu do Campo de Marte por volta das 13h15 do dia 31 de dezembro, com destino a Ilhabela, com o piloto e três passageiros. De acordo com as informações, além do piloto estavam no helicóptero Luciana Rodzewics, de 45 anos; a filha dela, Letícia Ayumi Rodzewics Sakumoto, de 20 anos; e Rafael Torres, um amigo da família que fez o convite para o passeio.
As buscas estavam sendo feitas pela Força Aérea Brasileira, Polícia Militar, Polícia Civil e o Corpo de Bombeiros de São Paulo. Durante as buscas, as equipes sobrevoaram a região da Serra do Mar, entre o litoral norte e o Vale do Paraíba, principalmente sobre as cidades de Paraibuna, Natividade da Serra, Redenção da Serra, Salesópolis e Caraguatatuba.
por Agência Brasil
O governo federal publicou um decreto prevendo a ampliação do número de vagas para cadastro de reserva do Concurso Nacional Unificado, chamado de Enem dos Concursos.
A norma que estabeleceu o certame previa que o quantitativo do cadastro de reserva seria o dobro da quantidade vagas. Pela nova regra, publicada na quarta-feira (10), a quantidade de vagas será definida em edital, com mais vagas do que o previsto anteriormente.

De acordo com o Ministério da Gestão e Inovação em Serviços Públicos, com o quantitativo anterior, muitos órgãos da administração pública enfrentariam dificuldade em preencher as vacâncias que acontecem ao longo do tempo.
A ministra da Gestão e Inovação em serviços Públicos, Esther Dweck, disse que com o novo decreto esse quantitativo poderá ser duplicado para cada bloco.
“Antes o cadastro de reserva era para um concurso específico. Então a regra de ter o dobro de aprovados funcionava. Nesse caso, um mesmo candidato poderá compor a lista de mais de um cargo. O que queremos garantir com a publicação desse decreto é que haja duas vezes o número de vagas de pessoas aprovadas naquele bloco”, explicou a ministra.
De acordo com o novo decreto, o limite de candidatos aprovados no certame será definido em edital e aqueles que não forem aprovados no quantitativo máximo estabelecido em edital, ainda que tenham atingido nota mínima, estarão automaticamente reprovados. Em caso de empate, o normativo aponta que nenhum dos candidatos empatados na última classificação de aprovados será considerado reprovado.
Na quarta-feira (10), o governo publicou os oito editais temáticos do certame, em edição extraordinária do Diário Oficial da União.
Outro ponto levantado pela ministra é o fato de que os aprovados no Concurso Nacional Unificado poderão, ser aproveitados, inclusive, em casos de excepcional necessidade de serviço público, como é o caso das contratações temporárias. Nesses casos, segundo a ministra, os candidatos convocados para as contratações temporárias continuarão na lista de espera para as contratações de cargo efetivo.
“Não faz sentido fazer concurso temporário, para uma contratação urgente, que vai levar o mesmo tempo de um concurso efetivo. Qual a lógica de você demorar quase um ano para contratar pessoas para algo que é urgente? O que queremos fazer é aproveitar os aprovados no banco de candidatos para as contratações temporárias. Para aqueles cargos que estão nos blocos, se algum dos órgãos precisar de temporário, poderá chamar os aprovados do banco de candidatos. Os candidatos convocados para as contratações temporárias continuam na lista de espera para as contratações de cargo efetivo”, informou a ministra.
O Ministério do Trabalho e Emprego atualizou a tabela anual do seguro-desemprego para 2024.
A correção levou em conta o Índice Nacional de Preços ao consumidor (INPC) de 2023, divulgado nesta quinta-feira (11) pelo Instituto Brasileiro de Geografia e Estatística (IBGE), que foi de 3,71%.

A nova tabela para os trabalhadores que tiverem direito ao benefício também entrou em vigor nessa quinta-feira (11).
Com isso, o valor do benefício seguro-desemprego não será inferior ao valor correspondente do salário mínimo vigente, R$ 1.412.
Já os trabalhadores que tenham recebido salários médios acima de R$ 3.402,65 terão direito, invariavelmente, ao seguro-desemprego no valor de R$ 2.313,74.
A portaria que reajusta em 3,71% os benefícios do Instituto Nacional do Seguro Social (INSS) acima de um salário mínimo foi publicada nesta sexta-feira (12) no Diário Oficial da União.

Com a definição do índice de reajuste – que segue o Índice Nacional de Preços ao Consumidor (INPC) do ano passado – o teto do INSS atual terá acréscimo de R$ 278,52, passando dos atuais R$ 7.507,49 para R$ 7.786,01 em 2024.
Além de corrigir os benefícios, o INPC também é aplicado para reajustar as contribuições para a Previdência Social, que sobem conforme o salário. Quanto mais o trabalhador na ativa recebe, mais está sujeito a alíquotas adicionais que elevam a contribuição.
Os benefícios atrelados ao salário mínimo subirão 8,4%, de R$ 1.320 para R$ 1.412. A variação corresponde à política correção aprovada em agosto do ano passado, que prevê a reposição da inflação pelo INPC do ano anterior, mais o crescimento do Produto Interno Bruto (PIB) de dois anos antes.
O decreto com o valor do salário mínimo, que responde pela maior parte dos benefícios da Previdência Social, foi assinado no fim de dezembro pelo presidente Luiz Inácio Lula da Silva.
O INSS começará a pagar os benefícios de janeiro no fim do mês. Para quem ganha um salário mínimo, o pagamento da aposentadoria, pensão ou auxílio será feito entre 25 de janeiro e 7 de fevereiro. Quem recebe além do mínimo terá o benefício depositado entre 1º e 7 de fevereiro.
Por - Agência Brasil








.jpg)
-PortalCantu-28-03-2026_large.png)
-PortalCantu-28-03-2026_large.png)




-PortalCantu-28-03-2026_large.png)
-PortalCantu-28-03-2026_large.png)







_large.jpg)