Pacientes oncológicas e representantes da Federação Brasileira de Instituições Filantrópicas de Apoio à Saúde da Mama (Femama) realizam nesta quarta-feira (9) manifestação, em frente ao Ministério da Saúde, em Brasília, em prol do acesso a tratamentos para a doença em estágio avançado e metastático via Sistema Único de Saúde (SUS) já aprovados, mas ainda não disponibilizados.

O objetivo, segundo a Coordenadora de comunicação da Femama, Mely Paredes, é sensibilizar a pasta apromover o acesso a medicamentos que já constam no Protocolo Clínico de Diretrizes Terapêuticas (PCDT) do câncer de mama, conhecido como PCDT Rosa, publicado em dezembro do ano passado.
“A função desse protocolo, a razão dele existir é que ele padroniza e regulamenta todas as linhas de cuidado do câncer de mama, com todas as medicações de cada linha de tratamento. A gente tinha medicações que tinham sido incorporadas em 2021 e 2022 para câncer de mama metastático e avançado que não eram disponibilizadas para os pacientes porque não tinha regulamentação”, explicou Mely.
A mobilização desta quarta-feira faz parte da campanha PCDT Rosa: quantos passos faltam?, que faz alusão à caminhada pelo acesso ao tratamento para câncer de mama, colocando em passos dados o tempo de aprovação e a disponibilização das terapias na rede pública.
“Em 5 de junho deste ano, completaram-se seis meses da publicação do documento e o acesso às medicações para tratamento de câncer de mama avançado e metastático ainda não acontece. O que acontece com essas pacientes? Não é que elas ficam sem tratamento. Elas recebem os tratamentos disponíveis dentro dos centros de saúde, mas que não são os mais adequados.”
Entenda
O Protocolo Clínico e Diretrizes Terapêuticas (PCDT) de câncer de mama, aprovado em dezembro de 2024, tem como objetivo otimizar o acesso ao diagnóstico e ao tratamento da doença no SUS, padronizando o cuidado e regulamentando a disponibilização de terapias.
Segundo a Femama, apesar da aprovação do documento, grande parte das mulheres com câncer de mama avançado e metastático em jornada oncológica na rede pública não têm acesso aos novos medicamentos incorporados, o que reduz a qualidade de vida e mesmo a taxa de sobrevida.
“Partindo da compreensão de que os marcos legais são apenas o início do percurso percorrido rumo ao pleno acesso ao diagnóstico precoce e tratamento adequado, a iniciativa da Femama destaca que a efetividade de uma política pública reside na disponibilização integral ao paciente de tudo aquilo que a regulamentação estabelece.”
Medicamentos
Em 2021 e 2022, duas portarias oficializaram a incorporação de inibidores de ciclina e da medicação trastuzumabe entansina no SUS. Para a Femama, os documentos representam os primeiros passos de uma longa caminhada. A partir das publicações, a entidade organizou a campanha PCDT Rosa: quantos passos faltam?, que remete a um percurso, similar aos aplicativos de caminhada e corrida, para mostrar o quanto já se caminhou desde a incorporação dos tratamentos.
Números
Dados do Instituto Nacional do Câncer (Inca) indicam que são esperados cerca de 74 mil novos casos anuais de câncer de mama no Brasil. A Femama destaca ainda que cerca de 75% da população brasileira, atualmente, depende exclusivamente do SUS.
“Ao se considerar que uma pessoa saudável caminha cerca de 7 mil passos por dia e que essa caminhada teve início em 2021, mais de 8,9 milhões de passos foram dados até o marco dos seis meses da publicação do PCDT, em junho de 2025, sem que a disponibilização igualitária dos novos medicamentos para as pacientes fosse uma realidade.”
Histórias
Cintia Cerqueira, 49 anos, trabalhava com confeitaria e artesanato até receber, em 2018, o diagnóstico de câncer de mama. No ano seguinte, a doença já havia atingido os ossos e o cérebro. Ao longo dos últimos sete anos, portanto, ela convive com um quadro de metástase – quando células cancerígenas se espalham de um tumor primário para outras partes do corpo, formando novos tumores em locais distantes.
Durante o período, Cintia passou por um total de três craniotomias, além de sessões de radioterapia na lombar e no fêmur. Para ter acesso aos medicamentos considerados mais adequados para o seu quadro, precisou acionar a Justiça. Ainda assim, passou cerca de oito meses aguardando para receber o tratamento indicado pelo oncologista.
"Eles cuidam daqueles que têm chance de ser curado, mas não cuidam dos que não têm chance de cura. Antes, eu não andava. Ficava mais deitada, não dava conta de varrer uma casa. Hoje, eu ando. Mudou minha vida completamente. A qualidade é outra. Tudo por causa da medicação”, contou.
“Dói mais que o câncer saber que existe um medicamento que pode te dar vida, mas que você não tem acesso. O que a gente quer é o mesmo direito que quem tem um câncer primário tem. Não porque somos melhores, mas porque não temos tempo pra esperar. Nossa luta é diária pra que os medicamentos sejam liberados.”
Por - Agência Brasil
A Agência Nacional de Vigilância Sanitária (Anvisa) publicou, nesta segunda-feira (7), um informe de segurança alertando sobre os riscos à saúde e aos cabelos relacionados ao uso de alisantes capilares, especialmente os que contêm substâncias proibidas, como o formol, ou formaldeído, e o ácido glioxílico. Os produtos irregulares podem causar desde irritações na pele até problemas respiratórios e danos irreversíveis à estrutura capilar. 

O documento destaca que, atualmente, o formol é permitido em produtos cosméticos no Brasil apenas como conservante, em concentrações de até 0,2%, e como endurecedor de unhas, até 5%. Seu uso como agente alisante é proibido e representa sérios riscos à saúde.
A Anvisa chama a atenção que “o ácido glioxílico, também proibido para essa finalidade, pode causar severos danos quando aquecido, sendo especialmente perigoso quando combinado com outros procedimentos, como a descoloração dos fios capilares”.
O informe traz orientações detalhadas para consumidores e profissionais de salões de beleza:
- consumidores devem verificar se o produto é regularizado junto à Anvisa;
- evitar produtos sem rótulo ou com promessas enganosas;
- seguir corretamente as instruções de uso;
- ficar atento a sinais como coceira, ardência ou dificuldades respiratórias.
Os profissionais devem utilizar apenas produtos regularizados e devem recusar o uso de substâncias proibidas, mesmo que a pedido do cliente. A Anvisa alerta ainda que os profissionais adotem medidas de proteção individual e mantenham os ambientes ventilados.
A Anvisa esclarece também que “a adição de formol a cosméticos é considerada infração sanitária grave e pode configurar crime hediondo, conforme o artigo 273 do Código Penal”.
A agência reforça a importância do monitoramento e da avaliação de produtos cosméticos após a sua comercialização para prevenir riscos e proteger a saúde pública.
Por - Agência Brasil
A síndrome pré-menstrual, popularmente conhecida como “TPM”, é um dos transtornos mais comuns enfrentados por mulheres em idade reprodutiva.
É um distúrbio clínico que ocorre na fase lútea do ciclo menstrual, durante os últimos 14 dias, e se encerra no início da menstruação. Desaparece até o quarto dia após a menstruação.
As causas podem estar ligadas às flutuações hormonais após a ovulação, dietas com carências nutricionais (especialmente em vitamina B6, magnésio e cálcio), histórico familiar, que inclui depressão ou ansiedade.
Caracterizada por sintomas físicos, emocionais e comportamentais, afetam o dia a dia das mulheres, diminuindo sua qualidade de vida.
Sintomas mais comuns:
- Sensibilidade nas mamas;
- Inchaço e ganho de peso;
- Dor de cabeça;
- Dores articulares e musculares;
- Acne;
- Alterações de humor como irritabilidade e tristeza;
- Ansiedade e/ou depressão;
- Alterações no apetite (comer em excesso)
Alimentos e nutrientes que podem aliviar ou prevenir os sintomas da TPM:
Carboidratos integrais
Durante a queda do estrógeno na fase lútea do ciclo menstrual, a produção de serotonina também diminui, gerando o aparecimento de sintomas emocionais.
O consumo adequado de carboidratos induz a produção de serotonina, podendo reverter os sintomas e melhorar o humor.
Os carboidratos devem compor cerca de 45 a 65% do valor energético da dieta, de preferência integral e evitar os refinados.
Fontes: arroz integral, aveia, quinoa, batata, aipim e milho.
/i.s3.glbimg.com/v1/AUTH_bc8228b6673f488aa253bbcb03c80ec5/internal_photos/bs/2025/k/y/q3BJknQKK0BSfV0yD8DA/alimentos-carboidratos.jpg)
Alimentos ricos em carboidratos — Foto: iStock
Alimentos ricos em triptofano
Além dos carboidratos, a produção de serotonina depende da ingestão do aminoácido triptofano.
Fontes: queijo, leite, oleaginosas e sementes, ovos, peixes, banana, abacate e chocolate.
Frutas, verduras e legumes
Possuem ação antioxidante e antiinflamatório, que podem reverter ou aliviar os sinais da TPM
Vitamina B6 - Piridoxina
Fonte alimentar: carne vermelha, frango, peixe, cereais integrais, legumes, batata, espinafre, banana, abacate, melancia, laranja, nozes e sementes.
Magnésio
Fontes: sementes (girassol, abóbora, linhaça, gergelim) , oleaginosas, cereais integrais (arroz, aveia, quinoa), folhosos verdes, leguminosas (feijão, lentilha, grão de bico, ervilha, soja), banana, abacate, figo, tofu.
Pesquisas indicam que o magnésio é eficaz para prevenir a TPM e a enxaqueca menstrual.
/i.s3.glbimg.com/v1/AUTH_bc8228b6673f488aa253bbcb03c80ec5/internal_photos/bs/2025/C/b/18dAsKQsiD0C6upHhAsQ/istock-1319902998.jpg)
Alimentos ricos em magnésio — Foto: iStock
Vitamina D e cálcio
Mulheres com dietas ricas em vitamina D e cálcio têm menor risco de desenvolver TPM.
Fontes de vitamina D: gema de ovo, salmão, sardinha, atum, tilápia, fígado, leite, queijo, manteiga, shitake. A principal fonte de vitamina D vem pela exposição ao sol, cerca de 20 minutos de exposição diária.
Fontes de cálcio: leite e derivados (queijos e iogurte), amêndoas, castanha-do-Pará, avelã, vegetais verde-escuros (brócolis, couve, espinafre) e peixes (sardinha, corvina, manjuba).
Quais alimentos evitar na síndrome pré-menstrual?
Enquanto alguns alimentos e nutrientes ajudam no alívio da síndrome pré-menstrual, outros podem exacerbar os sintomas. São eles:
- Sal;
- Açúcares;
- Gordura;
- Frituras;
- Cafeína;
- Álcool;
- Evitar fast-food e alimentos ultraprocessados;
Referências:
SIMINIUC, Rodica; TURCANU, Dinu. Impact of nutritional diet therapy on premenstrual syndrome. Frontiers in Nutrition, v. 10, p. 118, 2023.
Por - G1
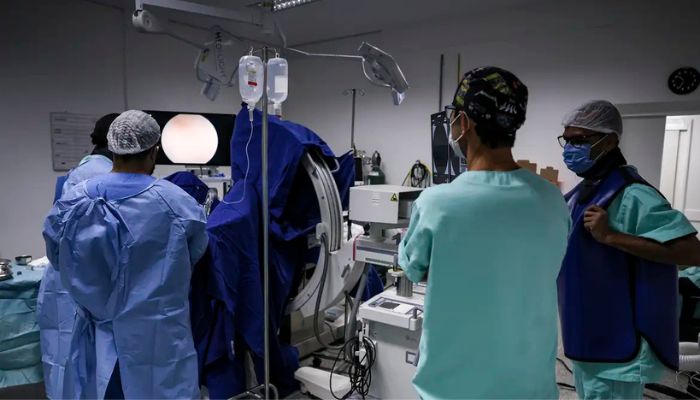
O mutirão Agora tem Especialistas Dia-E realizou de forma simultânea, em 24 estados brasileiros, mais de 1,1 mil cirurgias, além de 10 mil procedimentos, consultas e exames especializados, neste sábado (5), em 45 hospitais universitários federais administrados pela Empresa Brasileira de Serviços Hospitalares (Ebserh), em uma parceria dos ministérios da Saúde e da Educação.

O objetivo da iniciativa é ampliar a capacidade de atendimento da rede pública a fim de reduzir o tempo de espera por serviços especializados.
“É o maior mutirão do SUS já feito no Brasil inteiro e mais diverso. Já teve situação de fazer mutirão de uma cirurgia, [um tipo] de um procedimento. Hoje nós fizemos em todo o Brasil de Norte a Sul com 45 hospitais, que envolveram mil tipos diferentes de cirurgias, 10,3 mil procedimentos de diagnóstico, de consulta e é um movimento que não para hoje".
"Os hospitais universitários federais vão continuar fazendo mutirões, atendendo em terceiro turno os procedimentos de exames eletivos, não só urgência, para a gente reduzir o tempo de espera das cirurgias e dos exames em nosso país”, disse o ministro da Saúde, Alexandre Padilha, após visitar o mutirão no Centro Cirúrgico do Hospital Gaffrée e Guinle, da Universidade Federal do Estado do Rio de Janeiro (UNIRIO).
Prioridades
Padilha orientou que a prioridade dos atendimentos fosse aos pacientes oncológicos.
“A gente tem grande prioridade no câncer, porque no câncer tempo é vida. Fazer o diagnóstico o mais rápido possível, começar a cirurgia o mais rápido possível, pode significar a vida ou a morte daquele paciente”, observou.
Ainda segundo o ministro, em todo o país existem prioridades também para demandas que têm maior tempo de espera e impactam mais na população.
“São os problemas de saúde da mulher e toda a parte de ginecologia; a oncologia que é a parte do câncer; os problemas de visão, a gente envelhece cada vez mais e cada vez mais tem cirurgias e exames para tratar da visão; os problemas de ortopedia; de otorrino na parte da audição; são as grandes prioridades, além do câncer”, explicou.
Para o ministro é necessário acelerar o atendimento de saúde pública em todo o Brasil, mesmo em capitais que dispõem de mais médicos e hospitais. Ele citou um exemplo no Rio de Janeiro, onde foi identificado um paciente que esperava há dez anos para fazer uma cirurgia.
“Enquanto não vira urgência acaba não passando na frente de outros procedimentos e acaba ficando de lado. Essa ação do Agora tem Especialistas tem esse papel de identificar pacientes que estão há muitos anos esperando”, completou.
Atendimentos
O presidente da Ebserh, Arthur Chioro, destacou que os atendimentos do programa Agora tem Especialistas podem começar com a consulta médica. “É isso que mobiliza para que a gente possa ajudar esse esforço do Brasil de garantir – da consulta à cirurgia – as necessidades da população", comentou.
Chioro informou que em uma ação que começou em março foram feitas 89 mil cirurgias. Segundo ele, deve haver mais dois mutirões Dia-E até o fim deste ano, um em setembro e o outro em dezembro.
A orientação para os hospitais universitários federais, segundo Chioro, é para que ampliem o horário de funcionamento com um terceiro turno, incluindo atendimentos aos sábados e domingos.
“No nosso caso, na medida em que a gente aumentar a oferta de atendimento para a população, estamos envolvendo os novos alunos residentes, portanto, formando melhor os nossos futuros profissionais de saúde. É exatamente isso que diferencia o hospital universitário no compromisso com o ensino e a pesquisa, mas também com o SUS”, concluiu.
Parceria
A secretária de estado de Saúde do Rio de Janeiro, Claudia Mello, comemorou a parceria com os ministérios da Saúde e da Educação, porque também será acelerado o tratamento de pacientes do estado.
Segundo ela, quando se consegue verificar a fila interna de uma unidade é possível aumentar o acesso para novos pacientes chegarem ao sistema de saúde.
“A gente está avançando no país como um todo em 45 universidades no mutirão. É importante para nós do Rio de Janeiro e para o Brasil na diminuição de filas. Isso é o SUS avançando a cada dia”, pontuou.
Saúde da mulher
Antes da visita ao Hospital Gaffrée e Guinle, na Tijuca, zona norte do Rio, o ministro da Saúde esteve no mutirão do Hospital Universitário Clementino Fraga Filho, da Universidade Federal do Rio de Janeiro (UFRJ), na Ilha do Fundão e na sequência foi à maternidade Paulino Werneck, Ilha do Governador, zona norte da cidade.
Nos dois, estava acompanhado da primeira-dama, Janja Lula da Silva, da ministra da Igualdade Racial, Anielle Franco, e do presidente da Ebserh, Arthur Chioro. Lá, anunciaram medidas de reforço à saúde da mulher.
Por - Agência Brasil
Novo boletim InfoGripe, divulgado nessa quinta-feira (3) pela Fundação Oswaldo Cruz (Fiocruz), indica que os casos de Síndrome Respiratória Aguda Grave (SRAG) permanecem em alta na maior parte do país. A análise mostra indícios de queda ou interrupção do crescimento dos casos associados à influenza A em estados das regiões centro-sul, Norte e Nordeste e dos associados ao vírus sincicial respiratório (VSR) nas três regiões.

Nas últimas quatro semanas epidemiológicas, o índice de casos positivos foi de 33,4% de influenza A, 1,1% de influenza B, 47,7% de vírus sincicial respiratório, 20,6% de rinovírus e 1,8% de Sars-CoV-2 (covid-19). Entre os óbitos, a presença desses mesmos vírus foi de 74,1% de influenza A, 1,3% de influenza B, 14,1% de vírus sincicial respiratório, 10,2% de rinovírus e 3,1% de Sars-CoV-2 (covid-19).
A pesquisadora do InfoGripe Tatiana Portella diz que alguns estados ainda seguem com tendência de aumento de hospitalizações por SRAG - Mato Grosso, Paraná, Pará, Rondônia e Roraima. Ela ressalta que os maiores responsáveis por esse aumento continuam sendo a influenza A e o sincicial respiratório.
“Por isso, a gente reforça a importância da vacinação contra a influenza. O SUS [Serviço Único de Saúde] disponibiliza a vacina de graça para os grupos prioritários, então é fundamental que todos estejam vacinados. Mesmo que você já tenha tido gripe este ano, é importante se vacinar, já que a vacina protege contra os três principais tipos de vírus da influenza que infectam humanos”, recomenda a especialista.
Tatiana Portella acrescenta que a influenza A segue como a principal causa de hospitalizações e óbitos por SRAG entre os idosos. Segundo ela, a incidência de SRAG apresenta maior impacto nas crianças pequenas, estando associada principalmente ao VSR, seguido do rinovírus e da influenza A.
A pesquisadora lembrou que se verifica a interrupção do crescimento ou queda do número de casos de SRAG por influenza A na população de jovens, adultos e idosos, em parte significativa das regiões centro-sul, Norte e em alguns estados do Nordeste. Além disso, os casos de SRAG associados à Influenza A continuam aumentando em alguns estados do Nordeste, do centro-sul e em Roraima.
Estados
Um total de 6, das 27 unidades da Federação, apresenta incidência de SRAG em nível de alerta, risco ou alto risco, com sinal de crescimento na tendência de longo prazo, são eles: Alagoas, Mato Grosso, Paraná, Pará, Rondônia e Roraima. As ocorrências de SRAG na população de jovens, adultos e idosos, associadas à influenza A, se mantêm altas, mas apresentam sinal de queda no Distrito Federal, Espírito Santo,em Goiás, Mato Grosso do Sul, no Rio de Janeiro, Rio Grande do Sul, em Santa Catarina, São Paulo, no Amazonas, Amapá, Pará, em Rondônia, no Tocantins, na Bahia, no Ceará, Maranhão e na Paraíba. No entanto, continuam aumentando em Alagoas, Sergipe, Minas Gerais, Mato Grosso, no Paraná e em Roraima.
Por - Agência Brasil
O implante contraceptivo popularmente conhecido como Implanon será disponibilizado pelo Sistema Único de Saúde (SUS).
De acordo com o Ministério da Saúde, a opção é considerada vantajosa em relação aos demais contraceptivos em razão da longa duração — age no organismo por até três anos — e alta eficácia.

Em nota, a pasta informou que a decisão de incorporar o contraceptivo ao SUS foi apresentada na tarde desta quarta-feira (2) durante a reunião da Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec).
A portaria que oficializa a incorporação do contraceptivo deve ser publicada nos próximos dias. A partir da publicação, áreas técnicas da pasta terão 180 dias para efetivar a oferta, o que envolve etapas como atualização de diretrizes clínicas, aquisição e distribuição do insumo, capacitação e habilitação de profissionais, entre outras ações.
A previsão é que o medicamento esteja disponível em unidades básicas de saúde (UBS) a partir do segundo semestre. O plano, segundo o ministério, é distribuir 1,8 milhão de dispositivos, sendo 500 mil ainda este ano. O investimento será de cerca de R$ 245 milhões – atualmente, a unidade do produto custa entre R$ 2 mil e R$ 4 mil.
“Além de prevenir a gravidez não planejada, o acesso a contraceptivo também contribui para a redução da mortalidade materna, em alinhamento com os Objetivos de Desenvolvimento Sustentável (ODS) da ONU [Organização das Nações Unidas]”, destacou a pasta, ao citar o compromisso de reduzir em 25% a mortalidade materna geral e em 50% a mortalidade entre mulheres negras até 2027.
Entenda
O implante subdérmico Implanon é um método contraceptivo de longa duração e alta eficácia. Ele atua no organismo por até três anos, sem necessidade de intervenções durante esse período. Após o prazo, o implante deve ser retirado e, se houver interesse, um novo implante pode ser inserido imediatamente.
A inserção e a retirada do dispositivo devem ser realizadas por médicos e enfermeiros qualificados. Por esse motivo, segundo o ministério, a ampliação da oferta será acompanhada de estratégias de formação teórica e prática desses profissionais. Ainda de acordo com a pasta, a fertilidade é retomada rapidamente após a remoção.
Entre os contraceptivos oferecidos pelo SUS, apenas o DIU de cobre é classificado como Larc — sigla em inglês para contraceptivos reversíveis de longa duração. O método é considerado mais eficaz no planejamento reprodutivo por não depender do uso contínuo ou correto por parte da usuária, como ocorre com anticoncepcionais orais ou injetáveis.
“Os Larc são reversíveis e seguros”, destacou a pasta.
Confira, a seguir, os métodos contraceptivos disponíveis no SUS:
- preservativos externo e interno;
- DIU de cobre;
- anticoncepcional oral combinado;
- pílula oral de progestagênio;
- injetáveis hormonais mensal e trimestral;
- laqueadura tubária bilateral;
- vasectomia.
A pasta alertou que, entre todos contraceptivos disponíveis na rede pública, apenas os preservativos oferecem proteção contra infecções sexualmente transmissíveis (ISTs).
Por - Agência Brasil










_large.jpg)
_large.jpg)
_large.jpg)
_large.jpg)
_large.jpg)
_large.jpg)
_large.jpg)
_large.jpg)
_large.jpg)



